がんの最大の特徴は「不死」と「無限増殖」とが挙げられます。したがってがん治療は、がん細胞をアポトーシス(自然な細胞死)に導くこと、がんの増殖を止めること、この2つが重要なポイントです。がん細胞をアポトーシスに導くことと、増殖を止めることは同じようなことに思えるかもしれませんが、実際には異なるアプローチが必要となります。
従来の遺伝子治療はがんの「不死」と「無限増殖」に対して、どちらか一方にしか作用が認められないものも存在していましたが、昨今のがん遺伝子治療では「不死」と「無限増殖」のそれぞれに作用を示す治療タンパクを使用しています。
細胞の正常なサイクルを守るがん抑制遺伝子
正常細胞は細胞分裂とアポトーシス(自然な細胞死)により一定数を保っています。このような細胞の増殖やアポトーシス(自然な細胞死)を管理しているのが「がん抑制遺伝子」で、細胞のがん化を食い止め、がん化した細胞を死滅させるがん抑制遺伝子は本来私たちの体に備わっているしくみです。
がん細胞はがん抑制遺伝子が正常に働いていないため、異常な増殖を繰り返し、アポトーシス(自然な細胞死)を迎えることもありません。がんの発現には遺伝子の異常や欠如が大きく関係しています。
このような遺伝子の異常によりがん化した細胞に遺伝子を正常に導く「がん抑制遺伝子」を投与することにすることにより、がんの無限増殖をストップし、アポトーシス(自然な細胞死)を迎えさせるのが「がん遺伝子治療」です。
複数のがん抑制遺伝子でさまざまなアプローチ
治療タンパクを運ぶ役割をはたすものが、ベクターと呼ばれています。当初のがん遺伝子治療ではアデノウイルスというベクターを用いていました。しかし、このベクターは発現期間が短く、細胞の核に入り込む可能性も少ないことから、遺伝子治療のベクターとしては不十分なものでした。
近年のがん遺伝子治療では、より小さく改良された特殊なベクターを用いています。細胞の核にまで容易に入り込める特別な微小胞を用いたことによって、遺伝子治療は大きく前進しました。

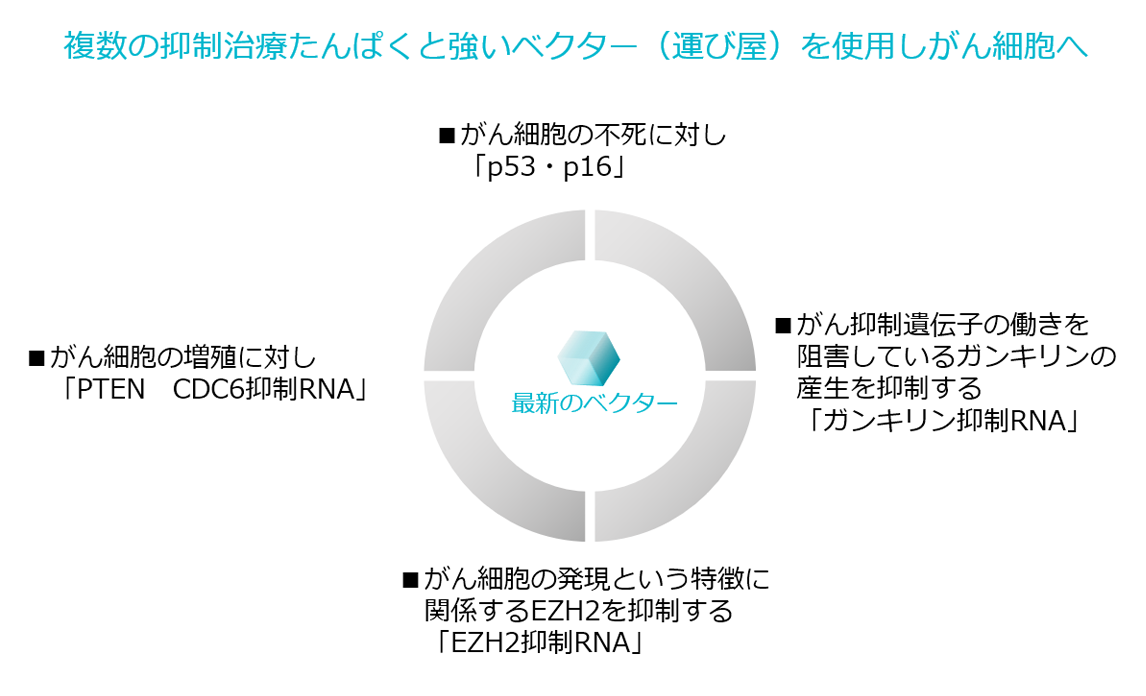
がん遺伝子治療はベクターを用いて、がん抑制タンパクをがん細胞内に半特異的に入り込ませ、がん細胞を自滅に追い込む治療です。このベクターに何を持たせて治療を行うのかは非常に重要です。がん遺伝子治療はなるべく多くのがん抑制遺伝子(p53,p16,PTEN,CDC6抑制RNA,EZH2抑制RNA,ガンキリン抑制RNA,GATA3,その他多種)をご状態に合わせ治療へ活用します。
- p53
-
p53は「ゲノムの守護神」と言われており、生まれてから死ぬまで体内の全ての細胞が30億の遺伝子情報を維持できるのはp53の働きによるものです。
p53は細胞分裂時のDNA修復の指示、またDNAの損傷が大きい場合における細胞死(アポトーシス)を指示するなど、DNAに傷を持っている細胞を制御する役割を担っています。
がんはp53の働きを抑制するためにMDM2というp53と結合するタンパクを多く産出したり、p53に対する抗体を作ったりしてp53がうまく働けないようにしてしまうため、がんに対して単純にp53を投与しただけでは、p53本来の効果を期待することはできません。そこで遺伝子治療では、MDM2やp53抗体になるべく反応しないようp53の改良を行った結果、本来の治療作用が得られるようになりました。
p53はDNAに傷をつける自滅促進型抗がん剤や放射線治療との相乗作用を示します。 - PTEN
-
PTENはがん患者さまのがん組織内における約50%(再発の患者さまにおいては殆ど)に機能障害が認められ、p53と同様代表的ながん抑制遺伝子です。通常PTENは細胞の増殖シグナルを脱リン酸化により遮断して細胞増殖を停止させることから、PTENはがんの激しい増殖に最も関与しているがん抑制遺伝子であるといえます。
PTENの働きが阻害されると、がんの増殖シグナルを遮断できなくなり、がん組織において血管新生が促進されてしまい、増殖因子が多く作られてしまう結果、がん細胞の増殖は加速されます。
このような状況に対しPTENの投与することで、細胞の増殖シグナル経路の途中の伝達物質を脱リン酸化させ増殖シグナルを遮断、がん細胞の過剰な増殖を阻害します。そして増殖阻害された細胞は細胞死を迎えます。
PTENはがん細胞の増殖シグナルを遮断することで増殖を抑制することから、同じ経路で働く増殖抑制型抗がん剤(分子標的薬やホルモン剤)と相乗作用を示します。 - p16
-
p16は細胞の老化に関係したがん抑制遺伝子で、細胞の異常な増殖を防ぎ、がんの発生を予防してくれます。そのため正常な細胞ではほとんど機能していませんが、老化していらない細胞には細胞分裂の周期中に分裂を遅らせ、異常細胞を排除する働きがあります。
p16はがん患者さまのがん組織内における約30%に(再発の患者さまにおいては殆ど)機能障害が認められ、特に喫煙者の肺がんなどでは非常に高い確率で欠損が認められます。
p16を投与することで、がんの新生血管形成が阻害されるほか、細胞分裂において一番重要な分裂期への移行に対してストッパーとしての役割もはたします。また、p16は他のがん抑制遺伝子が正常に機能できるように体内環境を作る役割も担っています。
p16は、がん細胞の増殖を抑制して自滅排除することから、抗がん剤との併用で相乗作用を示します。 - CDC6抑制RNA
-
CDC6は細胞を増殖させるために働くタンパク質で、細胞周期を調整する役割を持っています。通常は細胞周期の初期段階でCDC6が少量現れるのですが、ほとんどのがん細胞では周期などに関わらず、大量にCDC6が発現してしまい、がん細胞の増殖の元となる細胞分裂を増進させてしまいます。その結果、がん細胞が無限増殖するばかりか、がん抑制遺伝子の働きをも抑制してしまいます。
CDC6は正常な細胞分裂にも存在します。CDC6は30億の遺伝情報のCDC6を作る部分があり、そこをmRNAがコピーして細胞質でCDC6を作成します。がん細胞においてCDC6の製造が増加しているので、CDC6をつくるmRNAに反応させて(RNA干渉)、CDC6の生産を抑制させるCDC6抑制RNAを投与してCDC6産生を抑制させていきます。 - ガンキリン抑制RNA
-
ガンキリン抑制RNAはがん抑制遺伝子の働きを阻害するガンキリンの産生を抑制します。
ガンキリンとは1998年に京都大学医学研究科教授の藤田潤先生を中心に、ヒト肝細胞がんから発見された新規のがん遺伝子です。がん遺伝子の一種で、がん抑制遺伝子が作るがん抑制タンパクの多くを阻害、死滅へと導き、多くのがん遺伝子を促進させるがん遺伝子タンパクです。ガンキリンはがん抑制遺伝子の働きを阻害する目的として働きつづけ、がんの転移、浸潤、増殖、などがん細胞の働きに関わりがあることが認められています。腫瘍抑制因子を死滅させる作用があり、抑制遺伝子が機能しないため、がん細胞においては非常に重要な役割を持っています。
ガンキリン抑制RNAはp53やp16、PTEN、RBといった有名ながん抑制遺伝子の働きを妨げているガンキリンをターゲットとしたRNA標的で、ガンキリンの発現を抑えることにより、がん抑制遺伝子が本来の働きを取り戻し、効率的にがん細胞の消滅へ促進します。
ガンキリンを抑制することで、従来の遺伝子治療が前進することになりました。 - EZH2抑制RNA
-
EZH2は、細胞を発現させるために働くタンパク質で、がん細胞などの発現にも大きく関与しています。EZH2が多量に存在するがんは発現力が強く進行も速いため予後の悪いがんとなります。この発現に関与するEZH2もCDC6同様に正常な遺伝情報からmRNAのコピーで作られます。そのためEZH2を作るmRNAに働く、EZH2抑制RNAを投与しRNA干渉を利用してEZH2の産生を抑制させます。
EZH2を抑制させることは進行の早いがんや再発予防に重要な働きをします。
現在EZH2を抑制させる抗がん剤が研究開発されています。
安全性と効果を追求
がん細胞の核のなかに入り込み、それぞれの役目を果たしながらいくつもの経路を動かして、最終的には細胞の分裂を止めがん細胞をアポトーシス(自然な細胞死)に追い込んでいくのです。がん抑制遺伝子はいずれも相互に関連しあい、どれかひとつのみで働くということはありません。相互に協力し合いさまざまなアプローチで「がん」に対抗するのです。
がん細胞へ到達させる努力
使用する治療タンパクはp53,p16,PTEN,CDC6抑制RNA,EZH2抑制RNA,ガンキリン抑制RNA,GATA3など多数あり、オリジナルの治療が実現できるようになりました。ベクターも高分子ミセル化にて、大きさを80nm~100nm前後にして、完全に病原性を排除し、がん細胞内に半特異的に入り込む発現期間が長いものを使用しています。このようにがん細胞へ到達させるため、遺伝子治療は様々な努力によって進化し続けています。
- 高分子ミセル化
-
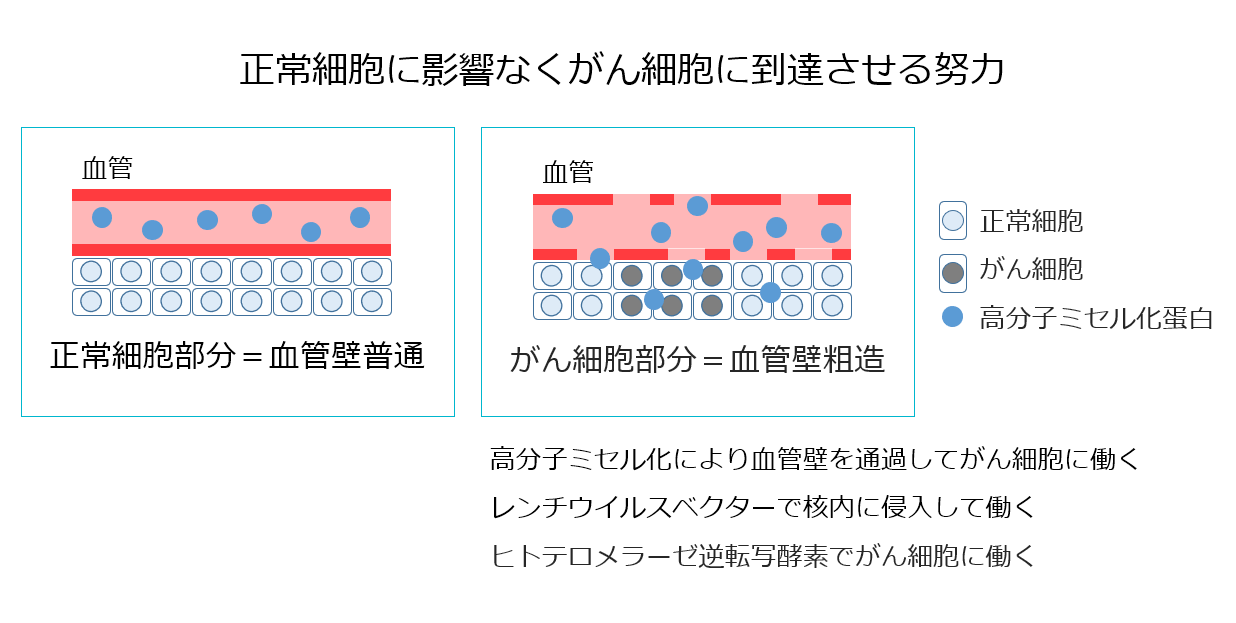
正常な血管は通過せず、粗造ながん血管壁だけ通過する大きさ(80nm~100nm前後)に整えて、がんへの到達率を高めます。(ドラックデリバリーシステム=DDS)
この大きさにすることを高分子ミセル化といい、現在抗がん剤もこの大きさに変える研究がされています(開発されればがんへの高い到達率をもつ副作用の少ない抗がん剤となる)。 - ヒトテロメラーゼ逆転写酵素(h-TERT)を利用
- 細胞分裂の時、DNAの転写はテロメアという部分から始められます。テロメアは分裂するたびに削られていき、無くなったら細胞は死を迎えます。そのためテロメアは「細胞の死の回数券」とも呼ばれています。しかし、がん細胞や幹細胞は無限にテロメアを作る、ヒトテロメラーゼという酵素を持っています。がんや幹細胞はこのテロメラーゼによって無限にテロメアを作ることができるため、無限に分裂することができます。この特徴を利用してヒトテロメラーゼ逆転写酵素(h-TERT)を付けることによって、がん細胞の中で半特異的に反応させます。
- 非ウイルス性(特徴は特別な微小胞)ベクター
-
病原性を完全に排除した上、安全性をさらに高めるため、特別な微小胞の性格のみを生かした非ウイルス性ベクターの開発に成功しました。これにより、がん抑制遺伝子をがん細胞内に半特異的に入り込ませ、長期発現することが可能となりました。
高分子ミセル化でがんへの到達率を高め、h-TERTでがん細胞に半特異的に反応させ、特別な微小胞の性格を生かしがん細胞内に入り込ませ、がん抑制遺伝子を届けるという仕組みです。
ベクター(運び屋)が重要
がん遺伝子治療はがん細胞の増殖を止める働きや、アポトーシス(自然細胞死)に導く複数のがん抑制遺伝子をベクターと呼ばれる高分子ミセル化させた運び屋に乗せて、がん特有の血管壁の粗造を利用してがん腫瘍まで持ち込み、がん細胞が特有にもつテロメラーゼを利用して半特異的にがん細胞内で反応させ、特別な微小胞の特性でがん細胞内に入り込みます。
またがん細胞にがん抑制遺伝子が到達すると、がん細胞の異常な増殖が抑制され、やがてアポトーシス(自然細胞死)を迎えます。
昨今の遺伝子治療ではより改良した特殊なベクターを使用しています。
- ベクターを高分子ミセル化することによって、正常な血管は通過せず、粗造ながんの血管壁だけを通過する大きさ(100nm前後)に揃えています(ドラックデリバリーシステム=DDS)。
- がんや幹細胞が持っている無限に増殖できるヒトテロメラーゼ。これに反応するヒトテロメラーゼ逆転写酵素を付けることで半特異的にがん細胞の中で反応させています。
- 特殊なベクターでがん細胞内に半特異的に入り込み、がん抑制遺伝子を侵入させ長期発現させています。
このように進化するベクターでがん抑制遺伝子やマイクロRNA抑制タンパクをがん細胞に到達させています。
がん細胞の特徴を理解し遺伝子レベルでがんを抑え込む働き
がんは「無限増殖」「不死」の状態。
➡ がん遺伝子治療はがんの原因である遺伝子異常を改善。
ほとんどのがん組織においてがん抑制遺伝子の機能が低下。
➡ がん遺伝子治療はこのようながんの原因となるがん抑制遺伝子を投与。
p53,p16,PTEN,(GATA3)
がんにおいて増えるとよくない蛋白(がんを増殖し促進させるCDC6,がんの発現に関係するEZH2,がん抑制機能を阻害するガンキリン)などがあり、これらを作るmRNAが増加。
➡ がん遺伝子治療はこのmRNAを抑制するRNA(CDC6抑制RNA,EZH2抑制RNA,ガンキリン抑制RNA)を投与します。
がん遺伝子治療もそれぞれに働く複数の治療蛋白と、がん細胞へ到達させる努力が必要となります。









